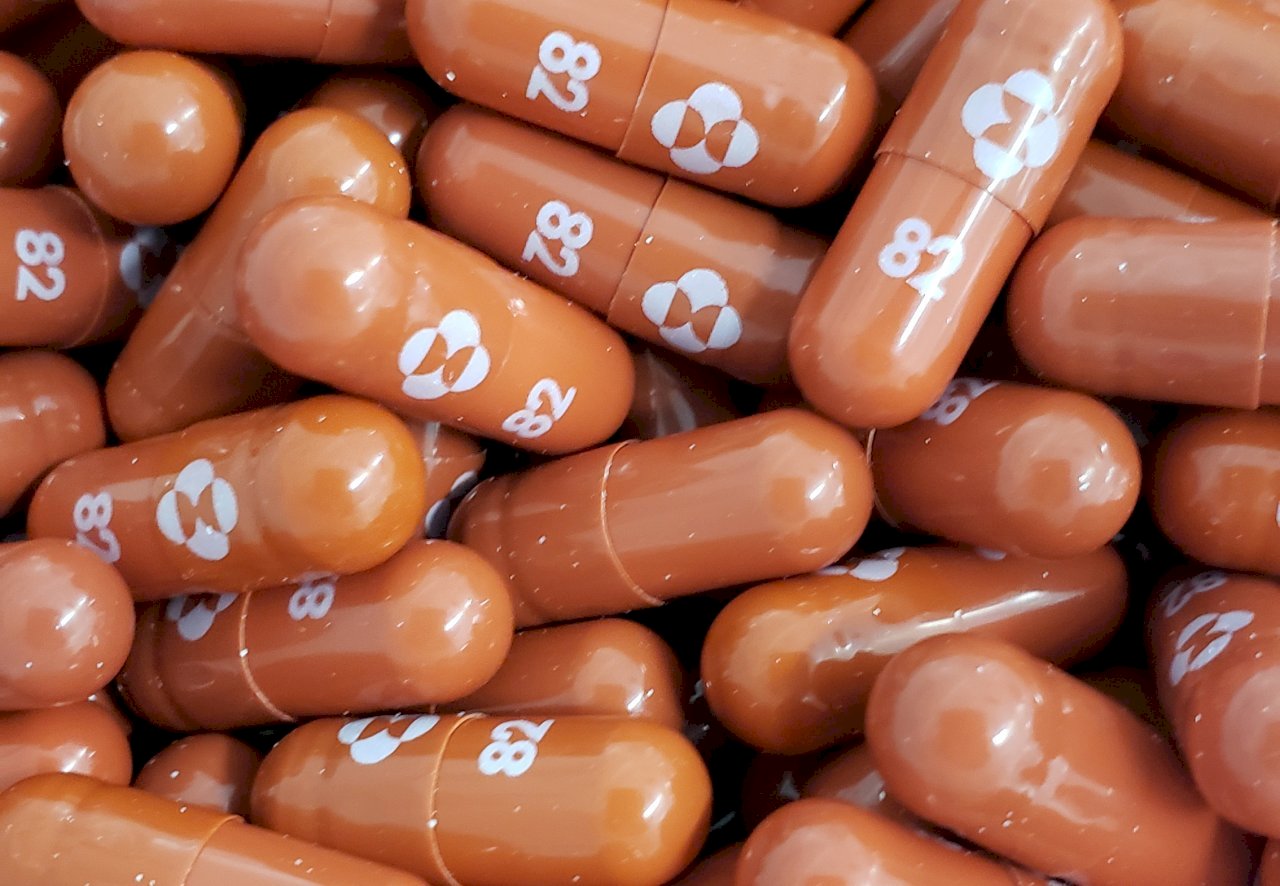
Ngày 11/10 hãng dược Merck& Co (Mỹ) cho biết, đã nộp đơn lên Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) xin cấp phép sử dụng khẩn cấp thuốc uống dạng viên molnupiravir để điều trị bệnh nhân mắc COVID-19 ở mức nhẹ đến trung bình. Nếu thuốc uống molnupiravir được FDA cấp phép sẽ trở thành loại thuốc uống điều trị COVID-19 đầu tiên được cấp phép sử dụng khẩn cấp.
Khi Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) cấp phép sử dụng khẩn cấp thì sẽ giúp thay đổi việc điều trị lâm sàng COVID-19 vì thuốc uống molnupiravir có thể được sử dụng tại nhà, qua đó nhằm giảm các triệu chứng và tăng tốc độ bình phục.
Theo báo cáo của hãng dược Merck công bố hồi đầu tháng cho thấy Molnupiravir giúp giảm gần 50% nguy cơ nhập viện và tử vong ở người bệnh COVID-19 nhẹ và vừa. Đây là kết quả trong thử nghiệm lâm sàng đối với nhóm bệnh COVID-19 nhẹ và vừa do hãng dược thực hiện.
Hãng dược Merck và đối tác Ridgeback Biotherapy cùng nghiên cứu phát minh ra thuốc điều trị COVID-19 Molnupiravir, cho biết đã nộp đơn xin cấp phép sử dụng khẩn cấp loại thuốc trên cho người lớn mắc COVID-19 từ nhẹ đến trung bình có nguy cơ mắc bệnh nặng hoặc phải nhập viện. Một loại thuốc viên dạng uống như Molnupiravir sẽ thuận tiện hơn trong điều trị bệnh nhân COVID-19, đặc biệt là bệnh nhân ngoại trú.
Hãng dược Merck& Co đã ký kết với chính phủ Mỹ hợp đồng cung cấp 1.700.00 liệu trình thuốc điều trị COVID-19 Molnupiravir với giá 700 USD cho một liệu trình điều trị bệnh COVID-19. Hãng dược Merck& Co dự tính đến cuối năm 2021 sẽ sản xuất 10 triệu liệu trình thuốc Molnupiravir.
Tố Kim







